Reacciones
de los alcanos
Los alcanos por lo general no se consideran sustancias muy reactivas.
Sin embargo, en condiciones adecuadas pueden llevar a cabo diversas
tipos de reacciones, incluyendo la combustión. El quemado del gas
natural, de la gasolina
y del petróleo implica la combustión de los alcanos. Todas estas reacciones son altaríiente exotérinicas:
Éstas, y reacciones similares, se han usado por mucho tiempo en
procesos industriales y en la calefacción doméstica y para cocinar.
La
halogenación de los alcanos -esto es, la sustitución de uno o más
átomos de hidrógeno por átomos de halógeno- es otra clase de reacción
bien estudiada. Cuando una mezcla de metano y cloro se calienta a más de
100ºC o se irradia con luz de longitud de onda apropiada, se produce el
cloruro de metilo:
Si el cloro gaseoso está presente en cantidad suficiente, la reacción puede continuar:
Una buena parte de la evidencia experimental sugiere que la etapa
inicial de la primera reacción de halogenación se lleva a cabo de la
siguiente
manera:
Así el enlace covalente del Cl2 SC rompe y se forman dos átomos de cloro. Se sabe que el enlace
Cl-Cl se rompe cuando se calienta o irradia la mezcla porque la energía de enlace del
Cl2 es 242.7 kJ/mol, mientras que se requieren unos 414 kJ/mol para rormper los enlaces C-H del
CH4.
Un
átomo de cloro libre contiene un electrón desapareado, que se ve como
un punto solo. Estos átomos son sumamente reactivos y atacan las
moléculas de metano de acuerdo con la ecuación:
Esta reacción produce cloruro de hidrógeno y el radical
Metilo ·CH3. El radical metilo es otra especie reactiva; se combina con el cloro molecular para dar cloruro de metilo y un átomo de cloro:
En la
misma forma se pueden explicar la producción de cloruro de
metilieno y las reacciones subsecuentes a partir del cloruro de metilo.
El mecanismo real es más complejo que el esquema que se ha mostrado
porque a menudo se producen "reacciones secundarias" que no conducen a
los productos deseados, como:
Los alcanos en los que se han sustituido uno o más átomos de hidrógeno por un átomo de halógeno se llaman
alqui halogenuros. Entre el gran número de alqui halogenuros, los mejor conocidos son el cloroformo
(CHCl3), el tetracloruro de carbono (CCl4), el cloruro de
metileno (CH2Cl2), y los clorofluorohidrocarburos.
El cloroformo es un líquido volátil, de sabor dulce, se usó
por muchos años como anestésico. Sin embargo, en virtud de su toxicidad
-puede producir daño severo en el hígado, los riñones y el corazón- ha
sido sustituido por otro compuesto. El
tetracloruro de carbono, también una sustancia tóxica, sirve como
líquido limpiador, pues quita manchas de grasa de la ropa. El cloruro de
metileno se usa como disolvente para
descafeinar el café y removedor de pintura.
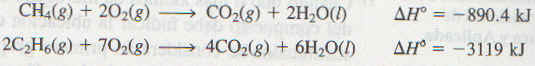


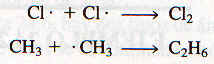
No hay comentarios:
Publicar un comentario